植物の光受容体には、フィトクロム(赤色光・遠赤色光)、クリプトクロム(青色光)、フォトトロピン(青色光)の3種が知られる。これらのうちクリプトクロム以外は、植物に特有の光受容体である。

(Furuya & Song, 1994より改変)
* フィトクロム
<フィトクロムの発見>
Borthwickらは、レタスの種子発芽誘導において、赤色光と遠赤色光がそれぞれ、促進的、阻害的に働くことを見出した。さらに、これらの光を交互に照射したときに、発芽への効果は最後に照射した光の波長で決まることを見出し、赤色光吸収型と遠赤色光吸収型の間を光変換する色素を提唱した(Borthwick et al., 1952)。これが有名な赤・遠赤色光光化逆性の発見である。
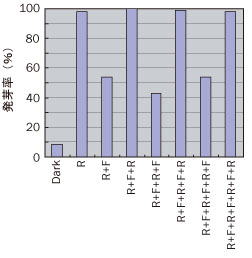
図: フィトクロムによる赤/遠赤色光可逆的発芽誘導
(Borthwick et al., 1952より改変)
Butlerらは、赤色光吸収型と遠赤色光吸収型の間を光変換するタンパク性の色素がトウモロコシの黄化芽生えに含まれること見出した(Butler et al., 1959)。これが植物に特有の光化逆的な光受容体「フィトクロム」の発見である。フィトクロムは陸上植物にのみ存在すると考えられていたが、最近、シアノバクテリアを中心にフィトクロム様タンパク質が多数発見された。 フィトクロムは、上に挙げた植物の光応答のうち、光屈性を除く全ての応答において主要な光受容体として働いている。
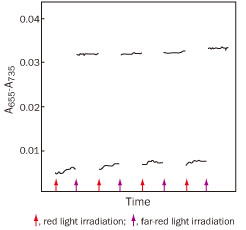
図: フィトクロム・タンパク質のPr-Pfr可逆的光変換
(Butler et al., 1959より改変)
<フィトクロムの分子構造>
フィトクロムは単量体分子量約11万の可溶性色素タンパク質で、発色団として開環テトラピロールであるフィトクロモビリンを1分子、システイン残基を介して共有結合している。フィトクロムは不活性型であるPr型で合成され、赤色光を吸収することにより活性型であるPfr型に変換される。また、Pfr型は遠赤色光を吸収することで不活性化されPr型に戻る。有名な赤/遠赤色光光可逆性はフィトクロムのもつこの性質の現れである。また、赤色光と遠赤色光の比率に応じてPfrとPrの間の光平衡が変化し、植物はこの変化を認識して避陰反応を引き起こす。
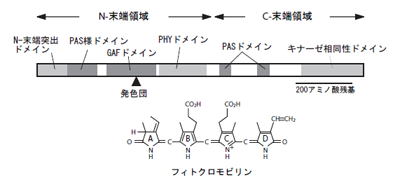
図: フィトクロムの一次構造の模式図
フィトクロムは比較的大きなタンパク質であり、大まかにN-末端側とC-末端側の2つの領域に分けられる。前者がフィトクロムの分光光学的活性を担っており、これのみで試験管ないでPr/Pfr間の光変換を示す。一方、後者は2量体化能と核移行活性をもつ。
フィトクロムのC-末端領域内には、PASドメインとキナーゼ相同性ドメインが見られる。これらのドメインが存在することから、フィトクロムのシグナルはC-末端領域から発信されると予想されていたが、N-末端領域のみを発現させても光受容体として機能することが判明した。フィトクロムのN-末端領域内には、さらに細かく、N-末端突出ドメイン、PAS様ドメイン、GAFドメイン、PHYドメインの4つの領域が認められる。発色団はGAFドメインに結合する。最近、バクテリオフィトクロム(後述)の一種でPAS-GAFドメインの結晶構造が明らかにされた。
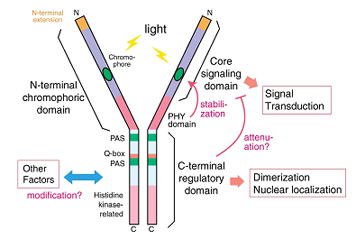
図:phyBの各ドメインの役割
<フィトクロムの分子種>
遺伝子レベルの研究が行われる以前より、フィトクロムには性質の異なる分子種が存在する可能性が指摘されていたが、1989年に、生化学的、分子生物学的な手法により、フィトクロムにはアミノ酸配列が異なり、別々の遺伝子にコードされた分子種が存在することが証明された。その後の研究によると、phyAとphyBはシダと種子植物の分岐の直後に分岐したと考えられる。
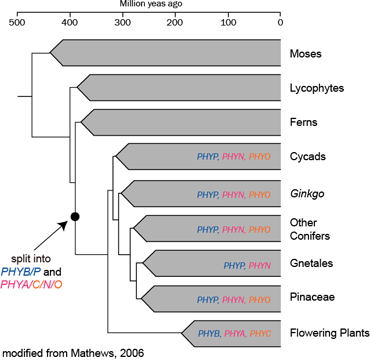
図: 陸上植物の進化過程におけるphyAとphyBの分岐
(Mathews, 2006より改変)
phyAとphyBの機能的な差は、その後の変異体を用いた研究により明らかとなった。phyAは暗所で高レベルに蓄積し、Pfr型に変換された後は速やかに分解される。また、連続遠赤色光への応答(遠赤色光高照射反応)や広い波長の微弱光への応答(超低光量反応)はphyAの働きによる。これらの応答は、低いPfrレベルで応答が起こる特殊な反応である。どのようにしてそれが可能となるのか、興味がもたれるが分子機構は不明である。一方、phyBは明暗にかかわらず一定量存在しPfr型が明所でも安定である。避陰反応はphyBの働きによる。
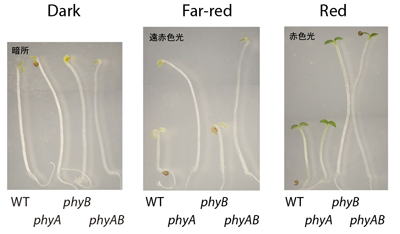
図: phyA欠損、phyB欠損、およびphyAphyB二重欠損変異体の芽生えの緑化
* フォトトロピン
<フォトトロピンの発見と分子構造>
フォトトロピンは1997年に米国のBriggsらのグループにより発見された青色光受容体である(Liscum et al., 1997)。その構造はクリプトクロムとは全く異なる。フォトトロピンは単量体分子量10万前後の色素タンパク質で、N-末端側にFMNを結合するLOVドメインを2つもち、C-末端側にはセリン/トレオニン・キナーゼドメインをもつ。このうちLOVドメインはバクテリアにも見られる。
LOVドメインはPASドメインの一種であり、FMNを結合し、光で励起されると、FMNとアポタンパク質の間に共有結合が形成される。このようにして形成された付加物は不安定で、暗所において自発的にもとの状態に戻る。付加物が結合した活性化状態では、LOV2ドメインの構造が変化しC-末端側のセリン/トレオニン・キナーゼが活性化される。すなわち、フォトトロピンは光によって活性化されるタンパク・キナーゼである。
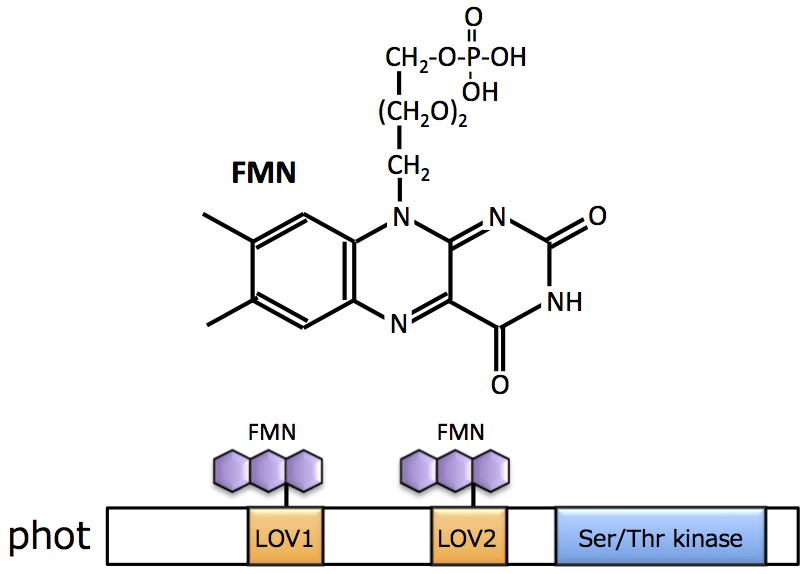
図: フォトトロピンの一次構造の模式図
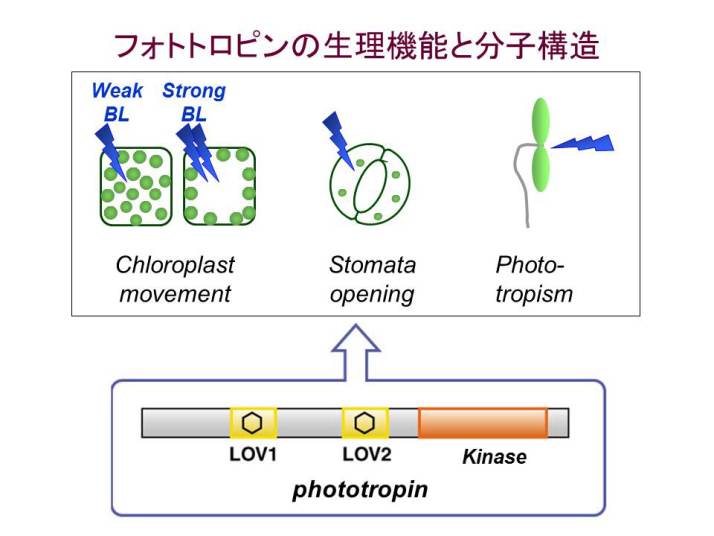
<フォトトロピンの生理応答>
フォトトロピンは光屈性の受容体として発見されたが、その後の研究で、葉緑体定位運動と気孔開口の光受容体でもあることが見いだされた。フォトトロピンにはphot1とpho2の二つが存在し、大まかには、phot1がより弱い光に、phot2が強い光に対する光受容体として働いている。
 * クリプトクロム
* クリプトクロム
クリプトクロムは1993年に米国のCashmoreらのグループにより発見された青色光受容体である(Ahamad et al., 1993)。その構造は生物界に広く存在する光回復酵素と相同性をもつ。植物での発見を契機として、動物にもクリプトクロムが存在することが示された。
クリプトクロムにはcry1とcry2の2つの分子種が存在する。cry1は脱黄化や明所での形態形成などに関わる。cry2は花芽形成を促進する主要な光受容体である。
研究の背景 topへ